Współczesna medycyna stoi na progu rewolucji, którą napędzają zaawansowane technologie analizy danych. Big data, czyli masowe przetwarzanie ogromnych zbiorów informacji, umożliwiło identyfikację nowych wzorców w danych medycznych, zwiększyło skuteczność diagnostyki oraz przyspieszyło rozwój terapii. Jednocześnie jednak wykorzystanie big data w badaniach klinicznych rodzi liczne dylematy etyczne, głównie dotyczące prywatności pacjentów, potencjalnej dyskryminacji oraz zgody na wykorzystanie danych. Czy korzyści płynące z analizy danych przewyższają zagrożenia związane z ich nadużyciem?
Era współczesna, często nazywana Wiekiem Informacji, nigdy nie bywa nazwana Wiekiem Wiedzy. Informacja nie przekłada się bezpośrednio na wiedzę. Musimy ją najpierw przetworzyć – dotrzeć do niej, przyswoić, zrozumieć, scalić z informacją już posiadaną i utrzymać. Robert B. Cialdini
Korzyści wykorzystania big data w badaniach klinicznych
1. Przyspieszenie odkryć naukowych i rozwoju terapii
Big data umożliwia analizę ogromnych zbiorów danych pochodzących z różnych źródeł, takich jak dokumentacja medyczna, wyniki badań laboratoryjnych czy dane genetyczne. Takie podejście pozwala naukowcom zidentyfikować wzorce, które mogą prowadzić do odkrycia nowych terapii lub predyspozycji do konkretnych chorób.
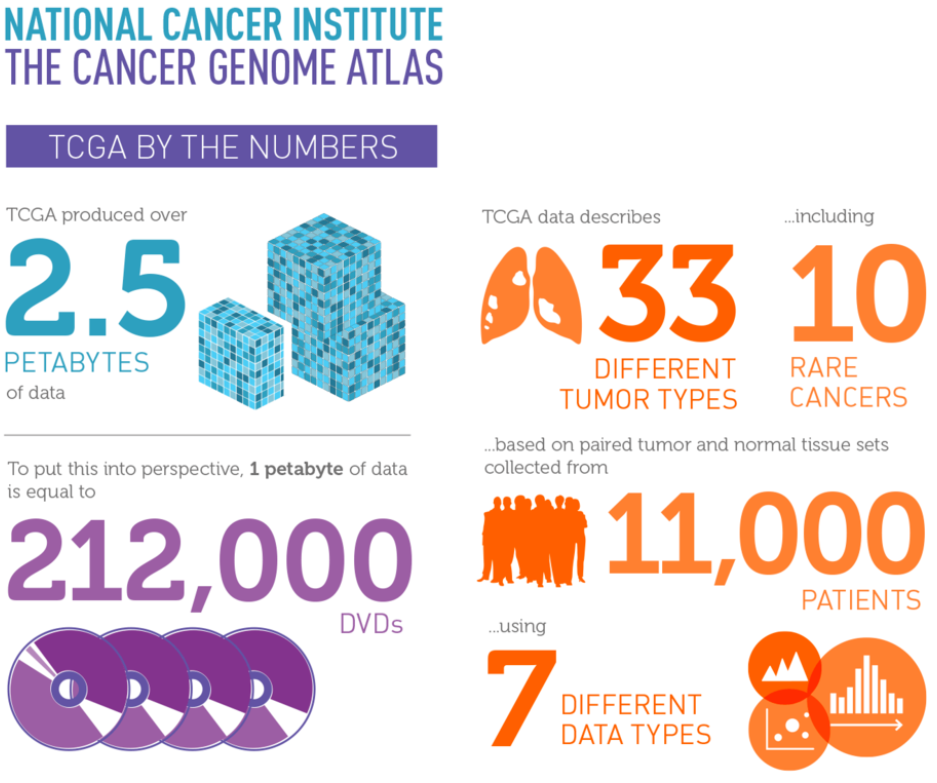
Jako przykład warto podać projekt Cancer Genome Atlas (TCGA), który wykorzystuje big data do analizy genomów pacjentów onkologicznych. Pozwoliło to na identyfikację nowych biomarkerów nowotworowych i opracowanie bardziej precyzyjnych terapii. Innym przykładem jest analiza danych z urządzeń wearable, takich jak inteligentne zegarki i sensory mierzące parametry zdrowotne pacjentów w czasie rzeczywistym. Dzięki temu naukowcy mogą monitorować efektywność leczenia i szybko identyfikować skuteczne schematy terapeutyczne.
W pandemii COVID-19 big data odegrało kluczową rolę w przyspieszeniu badań nad szczepionkami. Firmy farmaceutyczne, takie jak Pfizer i Moderna, wykorzystały algorytmy sztucznej inteligencji do analizy ogromnych zbiorów danych klinicznych, co pozwoliło na szybkie opracowanie i testowanie skutecznych preparatów.
Ponadto analiza big data przyczynia się do odkrywania nowych zastosowań istniejących leków. Przykładem może być wykorzystanie remdesiviru, pierwotnie opracowanego do leczenia wirusa Ebola, w terapii COVID-19, co było możliwe dzięki analizie danych klinicznych z różnych źródeł.
2. Medycyna personalizowana
Dzięki analizie big data możliwe jest dostosowanie terapii do indywidualnych potrzeb pacjenta. Algorytmy sztucznej inteligencji analizują historię choroby, styl życia oraz dane genetyczne, co pozwala na precyzyjne dobranie leczenia. Medycyna personalizowana zwiększa skuteczność terapii i zmniejsza ryzyko skutków ubocznych.
Przykładem zastosowania medycyny personalizowanej jest onkologia precyzyjna. W leczeniu nowotworów stosuje się analizy genetyczne w celu określenia mutacji odpowiedzialnych za rozwój raka. Na podstawie tych danych lekarze mogą dobrać terapię celowaną, która jest skuteczniejsza i mniej inwazyjna niż tradycyjne metody leczenia, takie jak chemioterapia.
Dodatkowo, spersonalizowana medycyna znajduje zastosowanie w diabetologii, gdzie inteligentne algorytmy analizują poziom glukozy we krwi, dietę oraz aktywność fizyczną pacjenta, dostosowując dawkowanie insuliny w czasie rzeczywistym, co znacznie poprawia kontrolę choroby i jakość życia pacjentów.
3. Poprawa skuteczności badań klinicznych
Analiza danych w czasie rzeczywistym pozwala na szybszą identyfikację skutecznych terapii oraz eliminację nieskutecznych metod leczenia. Zmniejsza to czas i koszty badań klinicznych, co ma kluczowe znaczenie zwłaszcza w przypadku opracowywania nowych leków.
Etyczne wyzwania
1. Ochrona prywatności pacjentów
Zapewnienie ochrony prywatności pacjentów jest kluczowym wyzwaniem w kontekście wykorzystania big data w medycynie. Chociaż stosowane są zaawansowane techniki anonimizacji, istnieje ryzyko ponownej identyfikacji pacjentów poprzez łączenie różnych zbiorów danych. Dlatego niezbędne jest wdrażanie skuteczniejszych metod zabezpieczeń oraz regulacji prawnych.
2. Zgoda pacjentów na przetwarzanie danych
Wielu pacjentów nie zdaje sobie sprawy, w jaki sposób ich dane są wykorzystywane. Brak przejrzystości w tej kwestii rodzi dylematy etyczne związane z uzyskaniem świadomej zgody na przetwarzanie danych medycznych. Konieczne jest opracowanie klarownych i zrozumiałych formularzy zgód oraz systemów pozwalających pacjentom na bieżące zarządzanie swoimi danymi.
3. Potencjalna dyskryminacja
Algorytmy analizujące big data mogą nieświadomie utrwalać istniejące nierówności społeczne i zdrowotne. Istnieje ryzyko, że systemy decyzyjne w ochronie zdrowia będą traktować osoby należące do określonych grup społecznych w odmienny sposób. Aby przeciwdziałać temu zjawisku, konieczna jest stała kontrola algorytmów oraz wprowadzanie mechanizmów eliminujących potencjalne biasy.
Ramy prawne i regulacje
Aby zminimalizować zagrożenia związane z big data w medycynie, wprowadzono regulacje prawne, takie jak RODO (Ogólne Rozporządzenie o Ochronie Danych) w Unii Europejskiej czy HIPAA (Health Insurance Portability and Accountability Act) w USA. Mają one na celu zapewnienie bezpieczeństwa danych oraz świadomej zgody pacjentów na ich przetwarzanie.
RODO nakłada na podmioty przetwarzające dane medyczne obowiązek wdrożenia środków technicznych i organizacyjnych w celu ochrony prywatności, takich jak minimalizacja danych, szyfrowanie oraz obowiązek informowania pacjentów o celach przetwarzania ich danych.
HIPAA natomiast reguluje przetwarzanie i ochronę informacji zdrowotnych w USA, określając standardy dotyczące poufności i integralności danych oraz zabezpieczeń przed ich nieautoryzowanym ujawnieniem.
Obie regulacje wspierają rozwój nowoczesnych technologii zabezpieczających dane pacjentów oraz stanowią podstawę do egzekwowania odpowiedzialności podmiotów zajmujących się przetwarzaniem danych medycznych.

Propozycje rozwiązań problemu
1. Wprowadzenie zaawansowanych technik anonimizacji
W dobie rosnącej ilości danych medycznych oraz ich kluczowej roli w badaniach i opiece zdrowotnej istotne jest zapewnienie odpowiedniego poziomu ochrony prywatności pacjentów. Tradycyjne metody anonimizacji, takie jak pseudonimizacja czy usuwanie danych identyfikacyjnych, okazują się niewystarczające w kontekście zaawansowanych technik analizy danych, które mogą umożliwić deanonimizację. W tej sytuacji nowoczesne technologie, takie jak federated learning oraz homomorficzne szyfrowanie, stają się kluczowymi narzędziami zapewniającymi wyższy poziom ochrony danych.
Federated learning pozwala na przeprowadzanie analiz i trenowanie modeli uczenia maszynowego bez konieczności przesyłania surowych danych do centralnych serwerów. Dane pozostają na urządzeniach użytkowników, a jedynie zaktualizowane wagi modeli są przesyłane do wspólnej sieci, co znacznie zmniejsza ryzyko naruszenia prywatności. Dzięki temu systemy oparte na federated learning mogą być wykorzystywane do analizy wrażliwych danych medycznych, takich jak wyniki badań diagnostycznych czy informacje o leczeniu, bez narażania pacjentów na ryzyko nieautoryzowanego dostępu do ich danych.
Jednym z kluczowych zastosowań tej technologii jest współpraca między placówkami medycznymi, które mogą wspólnie trenować modele AI na danych pacjentów bez konieczności ich centralizacji. Na przykład szpitale w różnych krajach mogą analizować trendy epidemiologiczne lub efektywność terapii, jednocześnie przestrzegając surowych regulacji dotyczących ochrony danych. Ponadto federated learning umożliwia personalizację modeli diagnostycznych w oparciu o lokalne dane pacjentów, co może poprawić precyzję wykrywania chorób, takich jak nowotwory czy choroby sercowo-naczyniowe, bez naruszania ich prywatności.
Z kolei homomorficzne szyfrowanie umożliwia wykonywanie obliczeń na zaszyfrowanych danych bez konieczności ich odszyfrowywania, co zapewnia wysoki poziom ochrony wrażliwych informacji medycznych. Implementacja tych rozwiązań może znacznie poprawić bezpieczeństwo przetwarzania danych pacjentów oraz ograniczyć ryzyko nieautoryzowanego dostępu.
2. Edukacja pacjentów
Wzrost świadomości pacjentów na temat wykorzystania ich danych oraz potencjalnych zagrożeń związanych z ich przetwarzaniem jest kluczowy dla budowania zaufania do systemu opieki zdrowotnej.
Jednym z kroków w tym kierunku jest organizowanie kampanii informacyjnych oraz warsztatów edukacyjnych, które przybliżą pacjentom zasady ochrony ich prywatności oraz sposoby korzystania z narzędzi umożliwiających kontrolę nad ich danymi. Istotnym elementem jest również uproszczenie i upowszechnienie informacji na temat polityki prywatności oraz możliwości wyrażania zgody na przetwarzanie danych, tak aby każdy pacjent miał świadomy wybór w tym zakresie.
Dodatkowo, wdrożenie intuicyjnych paneli użytkownika w systemach opieki zdrowotnej pozwoli pacjentom na łatwiejsze zarządzanie swoimi danymi, sprawdzanie, kto i w jakim celu uzyskuje do nich dostęp, oraz ewentualne cofnięcie zgód na określone operacje.
3. Transparentność algorytmów
Rosnące zastosowanie sztucznej inteligencji w analizie danych medycznych i podejmowaniu decyzji diagnostycznych wymaga szczególnej dbałości o transparentność stosowanych algorytmów. Niezrozumiałe i niekontrolowane modele decyzyjne mogą prowadzić do błędnych lub stronniczych decyzji, co może wpływać na jakość leczenia pacjentów oraz rodzić ryzyko dyskryminacji.
Aby zapobiec takim sytuacjom, konieczne jest wdrożenie mechanizmów audytu AI, które pozwolą na bieżącą kontrolę działania systemów i identyfikację potencjalnych biasów. Otwartość stosowanych algorytmów, publikowanie metod ich trenowania oraz prowadzenie niezależnych testów sprawdzających ich skuteczność i bezstronność są kluczowymi elementami budowania zaufania do AI w medycynie.
Kolejnym istotnym aspektem jest umożliwienie pacjentom oraz lekarzom śledzenia procesu decyzyjnego algorytmów, np. poprzez wizualizacje kroków analizy danych czy prezentowanie uzasadnień dla podjętych decyzji. Takie podejście nie tylko zwiększa transparentność systemu, ale również pomaga uniknąć potencjalnych błędów i nieporozumień w interpretacji wyników.
Wnioski
Big data w badaniach klinicznych to potężne narzędzie, które może przyspieszyć rozwój medycyny i poprawić jakość leczenia pacjentów. Jednak jego zastosowanie wiąże się z poważnymi wyzwaniami etycznymi. Kluczowe jest znalezienie równowagi pomiędzy postępem technologicznym a ochroną prywatności, co wymaga nie tylko regulacji prawnych, ale także zaangażowania wszystkich interesariuszy.
Bibliografia
- Weinstein, J. N., Collisson, E. A., Mills, G. B., Shaw, K. R., Ozenberger, B. A., Ellrott, K., … & Stuart, J. M. (2013). The cancer genome atlas pan-cancer analysis project. Nature genetics, 45(10), 1113-1120.
- Arshia Farmahini Farahani, Nika Kasraei (2024) Evaluating the Impact of Artificial Intelligence on Vaccine Development: Lessons Learned from the COVID-19 Pandemic.
- Sebastiani, M., Vacchi, C., Manfredi, A., & Cassone, G. (2022). Personalized medicine and machine learning: a roadmap for the future. Journal of clinical medicine, 11(14), 4110.
- Eghbali-Zarch, M., & Masoud, S. (2024). Application of machine learning in affordable and accessible insulin management for type 1 and 2 diabetes: A comprehensive review. Artificial Intelligence in Medicine, 102868.
- Brynjolfsson, E., & McAfee, A. (2017). Machine, Platform, Crowd: Harnessing Our Digital Future. W.W. Norton & Company.
- Mittelstadt, B. D., & Floridi, L. (2016). The ethics of big data: current and foreseeable issues in biomedical contexts. The ethics of biomedical big data, 445-480.
- Regulation, P. (2018). General data protection regulation. Intouch, 25, 1-5.
- Act, A. (1996). Health insurance portability and accountability act of 1996. Public law, 104, 191.